Buenas tarde a todos/as!! Como todos los días comenzamos con un vídeo para reflexionar, esta vez va sobre como a veces el no saber nos puede llevar a pensar de una forma equivocada. En mi opinión creo que todos/as deberíamos aprender constantemente e interesarnos por aprender.
Vídeo: Pi- pas
La materia 6
Mientras que las partículas en estado Sólido tienen un volumen fijo como podemos ver en la imagen las partículas en estado líquido están juntas pero con cierta distancia pero las partículas en estado sólido se encuentras más juntas.
¿Cómo podemos clasificar la materia?
Unas sustancias que se pueden separar por métodos más o menos sencillos y que sus propiedades dependen de la cantidad de cada componente, es decir no son fijas, a las que llamaremos mezclas.
Se hablará de mezclas en las que se distinguen sus partes, mezclas heterogéneas (agua y aceite,sal y limaduras de hierro….) y en las que no se distinguen, mezclas homogéneas, no se puede diferenciar los componentes ej: agua y sal; donde entran las disoluciones (agua y alcohol, agua y sale, el aire…)
Y otras que, o no se pueden separar (ej: el oxígeno y el hidrógeno obtenidos en la electrosis del agua) o sólo se pueden separar por reacciones químicas, y siempre tienen las mismas propiedades, que llamaremos sustancias puras. Las que ya no se pueden separar en otras (oxígeno, hidrógeno, oro, hierro… ) son sustancias puras simples y las que se pueden separar en otras, serán sustancias compuestas (agua, amoniaco, dióxido de carbono, cloruro sódico…).
Sustancias puras: No podemos separarlas (métodos sencillos) Dentro están: Simples,(elementos químicos) y compuestos (moléculas).
Simples: H, O, He, Al, Fe
Compuestos: CO2, H2O
Aquí os dejo un pequeño esquema que os ayudará a entender mejor la clasificación de las sustancias.
Aquí os dejo un pequeño esquema que os ayudará a entender mejor la clasificación de las sustancias.
A.24. Disponemos de una mezcla de arena de playa, sal común y limaduras de hierro.
Lo podemos separar con un embudo y a este le añadimos un papel de filtro.Se recoge el agua con sal y en el filtro se queda la arena. Calentamos(hervir) el agua con sal el agua se evaporará y quedarán unos cristales de sal en la superficie. También se pueden dejar el agua evaporarse a temperatura ambiente.
Tamización: separa materiales como el oro y la arena.
Filtración:
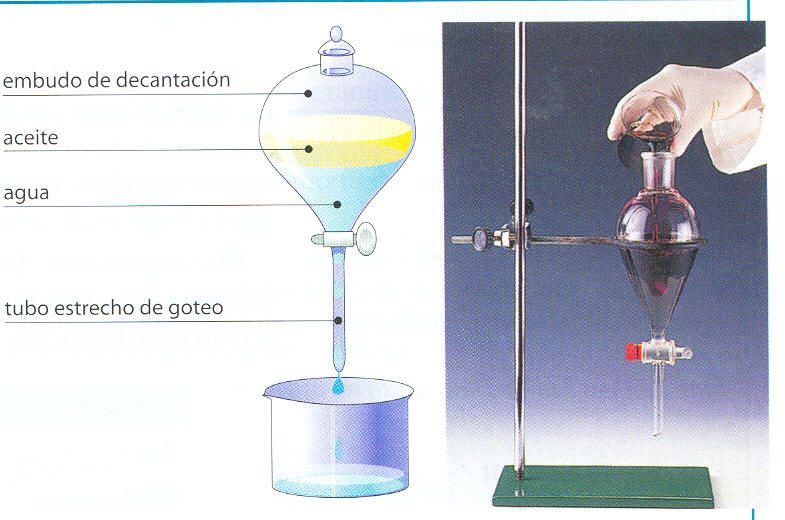
Decantación: Sólido-líquido (agua y arena, La arena se va al fondo y el agua queda encima, pasamos el agua a otro recipiente ) Líquido-líquido (agua y aceite, utilizamos un embudo de decantación. Cada líquido tiene diferente densidad por lo que el agua queda abajo y el aceite arriba, dejando caer el agua (gota a gota) quedándose el aceite.
Imantación:
Destilación: Calentando una bebida alcohólica llegamos a separar el alcohol del agua
el alcohol ebulliciona a unos 60g mientras que el agua necesita llegar a 100g.
Evaporación/ cristalización
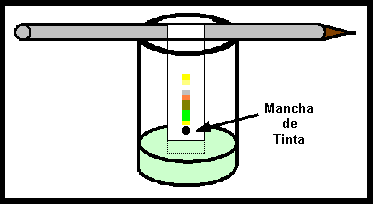
Cromatografía
A.25(power). Todos sabemos que el agua está formada por oxígeno e hidrógeno (H2O). ¿Se pueden separar el oxígeno y el anterior?¿Se te ocurre alguna forma de separar el oxígeno y hidrógeno del agua por un método como el de la actividad el hidrógeno del agua?
La forma de separación del hidrógeno y el oxígeno del agua. Los métodos de separación de mezclas no valen para compuestos químicos. es por una reacción química de electrolisis.
Por lo que ningún método sirve para separar el agua. Se trata de una sustancia pura (Método electrolisis).
2 H2O: 2 H2 + O2
A.26. Tenemos en un vaso un poco de alcohol etílico, otro con agua, un tercero con un poco de alcohol y un poco de agua y un cuarto con agua y aceite ¿Cómo podrías
distinguirlos? En el laboratorio no se puede probar ni oler nada, ya que existen sustancias tóxicas.
El de agua y aceite se distingue a simple vista, sus partes son visibles. Para los otros tres hay que llegar a las propiedades de cada uno de ellos.
Por ejemplo por el pto. de fusión y ebullición, por la densidad, por la
conductividad, …
Una vez medida alguna de esas propiedades se puede ir a una tabla y compararla para saber que sustancia es. Pero en las tablas aparece agua, alcohol etílico, …., pero NO aparece “un poco de alcohol y un poco de agua”
A.27. ¿Cómo puede explicarse la existencia de un centenar de sustancias simples y de millones de compuestos? Realizar dibujos explicativos.
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curs
o/materiales/clasif/clasifica1.htm
Para explicar la enorme diversidad de compuestos hay que pensar que estos se forman por la combinación de los simples. Igual que ocurre con el lenguaje, con sólo 28 letras se forman miles y miles de palabras. En la naturaleza, al combinarse los 100 elementos de la tabla periódica, se obtienen millones de compuestos distintos.





No hay comentarios:
Publicar un comentario